Фармакология, токсикология
УДК 619:615.015.4
DOI:10.12737/16667
Поступила в редакцию 06.07.2015
Принята в печать 24.11.2015
Скачать статью в PDF формате
English version
Влияние антигельминтика митранокса на гематологические и биохимические показатели крови крыс в субхроническом опыте
Козлов С. А., Мусаев М. Б.
Всероссийский научно-исследовательский институт фундаментальной и прикладной паразитологии животных и растений имени К. И. Скрябина 117218, Москва, ул. Б. Черёмушкинская, 28, e-mail: serg1vet@mail.ru, musaev@vniigis.ru
Реферат
Цель исследования – изучение влияния митранокса на гематологические и биохимические показатели крови крыс.
Материалы и методы. Опыт проводили на 40 беспородных белых крысах-самцах, разделенных на 4 группы по 10 крыс в каждой. Крысам первых трех групп вводили суспензию препарата, приготовленную на 1%-ном крахмальном геле, индивидуально перорально в дозах 1/5, 1/10 и 1/20 от ЛД50 (830,4 мг/кг) соответственно.Животные четвертой группы препарат не получали и служили контролем. Суспензию препарата задавали животным ежедневно в течение 7 сут. Убой животных проводили методом резекции яремных вен с последующей резекцией шейных позвонков. Кровь животных и внутренние органы исследовали в соответствии с общепринятыми методиками.
Результаты и обсуждение. Митранокс в дозах 1/5 и 1/10 от ЛД50 при даче в течение 7 сут вызывал у подопытных крыс повышение концентрации общего белка, уровня глюкозы, концентрация мочи в сыворотке крови, как и активность аспартат- и аланинаминотрансферазы, щелочной фосфатазы. Все это указывает, что препарат оказывает гепатотоксическое действие на крыс, вызывая угнетение гуморальных факторов неспецифического иммунитета. В дозе 1/5 от ЛД50 оказывает отрицательное воздействие на поджелудочную железу животных, повышая ее ферментативную активность.
Ключевые слова: антигельминтик, митранокс, субхроническая токсичность, гематологические и биохимические показатели крови.
Введение
Митранокс – новый отечественный препарат широкого спектра антигельминтного действия. Относится к группе ацетиллированных салициланнилидов [11]. Препарат представляет собой белый с кремовым оттенком порошок, без вкуса, в воде не растворим, молекулярная масса 377,06; предназначен для перорального применения; обладает цестодоцидным и нематодоцидным действиями [3]. Митранокс разработан совместно с СПХФА и ИМПИТМ им. Е. И. Марциновского и предоставлен для испытаний на животных проф. Ф. С. Михайлицыным.
По данным доклинических исследований митранокс в соответствии с ГОСТ 12.10007-76 относится к 3 классу умеренно опасных веществ по степени воздействия на организм при введении в желудок белым мышам и крысам [2]; по принятой классификации химических веществ обладает умеренным кумулятивным свойством (Ккум.= 3,2) [4].
По результатам изучения острой накожной токсичности он относится к классу малоопасных веществ, не оказывает отрицательного воздействия на неповреждённую кожу и не оказывает существенного раздражающего действия на конъюнктиву глаз [5, 6].
Учитывая относительную дешевизну синтеза митранокса, его слабую токсичность и широкую антигельминтную активность, целью работы было изучение влияния митранокса на гематологические и биохимические показатели крови крыс.
Материалы и методы
Изучение субхронической токсичности митранокса проводили в виварии Всероссийского научно-исследовательского института фундаментальной и прикладной паразитологии животных и растений им. К. И. Скрябина (ВНИИП) в соответствии с «Руководством по экспериментальному (доклиническому) изучению новых фармакологических веществ» [10], «Методическими указаниями по гигиенической оценке новых пестицидов» [7] и правилам лабораторной практики в Российской Федерации [1, 9].
В опыте было использовано 40 беспородных белых крыс-самцов. Животных распределили на 4 группы по 10 крыс в каждой по принципу аналогов. Перед началом опыта животных содержали на двухчасовой голодной диете.
Крысам первых трех подопытных групп суспензию препарата, приготовленную на 1%-ном крахмальном геле, задавали в течение 7 сут ежедневно индивидуально перорально с помощью специального внутрижелудочного зонда в дозах 166,08; 83,04 и 41,04 мг/кг (или 1/5, 1/10 и 1/20 от ЛД50, равной 830,4 мг/кг) соответственно. Животные четвертой группы препарат не получали и служили контролем.
На протяжении всего эксперимента за животными вели наблюдение. Обращали внимание на акт приема корма и воды, общее состояние животных, наличие признаков интоксикации. Взвешивание животных и регистрацию их массы проводили на 1, 3, 5 и 7-е сутки. Учитывали также их начальную массу.
На 8-е сутки опыта животных убивали декапитацией. У каждого животного брали кровь для биохимического и гематологического анализа.
После убоя крыс проводили лапаротомию с последующей экстирпацией и взвешиванием внутренних органов (сердце, легкие, печень, почки, селезенка, мозг, семенники, тимус, поджелудочная железа, надпочечники). При этом обращали внимание на наличие макроскопических изменений (цвет, форма, консистенция органов, наличие кровоизлияний).
Статистическую обработку данных проводили методом вариационной статистики с помощью простого сравнения средних значений по двустороннему t-критерию Стьюдента. Различие определяли при 0,05 уровне значимости. Расчет выполняли на компьютере с использованием приложения Microsoft Excel 2010 и пакета статистического анализа данных Statistica 8.0 for Windows.
Результаты и обсуждение
На протяжении всего эксперимента животные, получавшие препарат, охотно принимали корм и воду и визуально не отличались от животных контрольной группы. Признаков интоксикации (взъерошенность шерстного покрова, гипо- и адинамия, угнетение, диарея и т. д.) не отмечали.
Крысы всех групп динамично набирали массу. Средний прирост массы животных трех опытных групп полностью соответствовал приросту массы животных контрольной группы: соответственно 134,3±1,7; 134,3±1,90; 136,7±1,35 и 139,4±1,71. Средний прирост массы тела измеряли в процентах к исходной массе тела.
При макроскопическом исследовании внутренних органов опытных животных отклонений от нормы не выявлено. Внешний вид, форма и консистенция органов, масса органов и их массовые коэффициенты у опытных животных полностью соответствовали контролю (табл. 1).
Показатели крови крыс, которым задавали митранокс в дозах 1/5, 1/10 и 1/20 от ЛД50, не отличались от таковых у животных контрольной группы (табл. 2).
Не установлено существенного влияния препарата на биохимические показатели сыворотки крови у подопытных крыс, за исключением нескольких показателей (табл. 3). Митранокс в дозе 1/5 и 1/10 от ЛД50 вызывал повышение содержания общего белка в сыворотке крови крыс (соответственно до 87,87±1,01 и 89,26±1,24 г/л против 77,28±0,24 г/л в контроле).
Активность аспартат- и аланинаминотрансферазы у всех животных в испытанных дозах была повышена (328,61±16,77; 310,33±16,02; 336,58±15,05 и 80,54±4,75; 71,38±2,30; 74,55±1,11), т. е. препарат оказывает гепатотоксическое действие на крыс.
Активность щелочной фосфатазы в сыворотке крови животных была также повышена (628,70±29,76; 645,20±48,17; 618,90±34,61) по сравнению со контрольными животными (548,00±22,23), что свидетельствует о нарушении процессов гликогенеза и регенерации из-за негативного воздействия препарата.
Таблица 1
Значения массовых коэффициентов органов у крыс при пероральном введении в течение 7 суток
митранокса в трех дозах (n = 10)
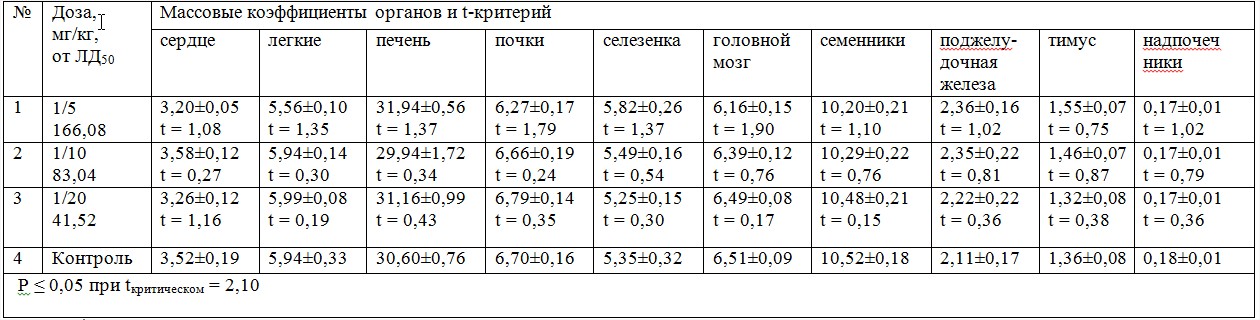
Таблица 2
Гематологические показатели крыс при пероральном введении в течение 7 суток митранокса в трех дозах (n = 10)
|
Показатель |
Значение показателя при введении митранокса в дозах, t-критерий |
||||||
|
1/5 от ЛД50 |
1/5 от ЛД50 |
1/5 от ЛД50 |
Контроль |
||||
|
Гематокрит, % |
57,38±0,45 t = 1,31 |
59,02±1,55 t = 1,64
|
59,32±3,10 t = 1,04
|
55,69±1,14 |
|||
|
Гемоглобин, г/л |
164,5±2,56 t = 1,92 |
165,7±5,07 t = 1,29
|
167,0±5,19 t = 1,49
|
158,5±1,51 |
|||
|
Эритроциты, 1012/л |
9,49±0,13 t = 2,00
|
9,67±0,29 t = 1,74
|
9,19±0,44 t = 0,21
|
9,1±0,12 |
|||
|
Сред. содержание гемоглобина в эритроците, пг |
17,6±0,14 t = 1,76 |
17,49±0,19 t = 0,76
|
17,27±0,10 t = 0,60
|
17,3±0,07
|
|||
|
Сред. концентрация гемоглобина в эритроците, % |
28,7±0,39 t = 2,01
|
29,01±0,51 t = 2,03
|
28,4±0,22 t = 1,97
|
27,98±0,18 |
|||
|
Средний объем эритроцита, мкм3 |
60,41±0,77 t = 2,07
|
60,58±0,69 t = 2,09
|
61,18±0,60 t = 1,57
|
62,3±0,35 |
|||
|
Показатель анизоцитоза эритроцитов, % |
16,23±0,26 t = 0,66
|
15,76±0,21 t = 1,92
|
15,8±0,22 t = 1,78
|
16,51±0,31
|
|||
|
Лейкоциты, 109/л |
7,75±0,87 t =1,67
|
6,2±0,35 t = 0,20
|
5,45±0,65 t = 0,71
|
6,04±0,44 |
|||
|
Тромбоциты, 109/л |
420,9±42,47 t = 0,10
|
432,9±17,93 t = 0,18
|
366,6±21,26 t = 1,54
|
426,2±29,9 |
|||
|
Лейкоцитарная формула |
|||||||
|
Сегментоядерные нейтрофилы, % |
36,7±3,05 t = 0,06
|
32,5±4,04 t = 0,70
|
33,4±4,78 t = 0,49
|
36,4±3,36
|
|||
|
Эозинофилы, % |
1,4±0,43 t = 0,34
|
2,00±0,52 t =1,21
|
1,20±0,51 t = 0
|
1,2±0,36 |
|||
|
Базофилы, % |
0
|
0
|
0
|
0
|
|||
|
Моноциты, % |
1,5±0,40 t = 1,41
|
1,90±0,28 t = 0,76
|
1,6±0,52 t = 0,99
|
2,2±0,25 |
|||
|
Палочкоядерные нейтрофилы, % |
0,60±0,22 t = 0,00
|
0,40±0,22 t = 0,55
|
0,8±0,33 t = 0,45
|
0,60±0,27 |
|||
|
Лимфоциты, %
|
61,3±3,52 t = 0,31
|
62,40±4,62 t = 0,44
|
62,6±4,40 t = 0,49
|
59,6±3,86 |
|||
|
Р ≤ 0,05 при tкритическом = 2,10
|
|||||||
Таблица 3
Биохимические показатели сыворотки крови у крыс при пероральном введении в течение 7 суток митранокса в трех дозах (n = 10)
|
Показатель |
Значение показателя при введении митранокса в дозах, t-критерий |
|||
|
1/5 |
1/10 |
1/20 |
контроль |
|
|
Билирубин общий, мкмоль/л |
3,19±0,16 t = 1,43
|
2,95±0,24 t = 1,91
|
2,97±0,26 t = 1,66
|
3,43±0,03
|
|
Билирубин прямой, мкмоль/л |
1,62±0,11 t = 0,08
|
1,42±0,13 t = 1,32
|
1,35±0,11 t = 2,04
|
1,61±0,07 |
|
АСТ, Е/л |
328,61±16,77* t = 2,28 |
310,33±16,02* t = 1,49 |
336,58±15,05* t = 2,84 |
278,93±12,02
|
|
АЛТ, Е/л |
80,54±4,75* t = 4,07 |
71,38±2,30* t = 4,13 |
74,55±1,11* t = 6,41 |
58,57±1,92 |
|
Коэффициент Ритиса |
4,15±0,22 t = 1,69 |
4,38±0,25 t = 1,08 |
4,58±0,19 t = 0,65 |
4,83±0,31
|
|
Мочевина, ммоль/л |
5,57±0,25 t = 2,07 |
5,32±0,31 t = 1,48 |
4,65±0,34 t = 0,23 |
4,52±1,67 |
|
Креатинин, мкмоль/л |
66,63±2,30 t = 2,06 |
66,3±2,44 t = 1,93 |
64,92±1,06 t = 1,96 |
58,81±2,76 |
|
Общий белок, г/л |
87,87±1,01* t = 9,59 |
89,26±1,24* t = 9,01 |
80,86±1,74 t = 1,93 |
77,28±0,24
|
|
Щелочная фосфатаза, Е/л |
628,7±29,76 t = 2,04
|
645,20±48,17 t = 1,73
|
618,9±34,61 t = 1,62
|
548,00±22,23 |
|
Альфа-амилаза общая, Е/л |
2948,18±57,80* t =4,68
|
3198,55±295,56 t = 2,01
|
3303,00±340,17 t = 2,04
|
2564,56±51,95 |
|
Глюкоза, ммоль/л |
6,52±0,29 t = 1,77 |
6,48±0,24 t = 1,97 |
6,47±0,18 t = 1,99 |
5,89±0,16
|
|
ЛДГ, Е/л |
4158,5±240,93* t = 4,14 |
3850,1±202,01* t = 3,49 |
4003,6±325,13* t = 2,75 |
3012,00±105,54 |
* Различие статистически достоверно между значениями показателей опытной и контрольной группами (Р ≤ 0,05 при tкритическом = 2,10)
Концентрация мочевины в сыворотке у подопытных животных была незначительно увеличена (5,57±0,25; 5,32±0,31; 4,65±0,34 против 4,52±1,67 ммоль/л в контроле), что свидетельствует о почечной недостаточности и нефротоксическом действии на организм крыс.
Уровень глюкозы у подопытных животных был слегка повышен (6,52±0,29; 6,48±0,24; 6,47±0,18 против 5,89±0,16 ммоль/л в контроле), что указывает на нарушение процесса гликолиза, сопровождающееся ростом концентрации глюкозы в сыворотке крови.
Таким образом, митранокс в дозах 1/5 и 1/10 от ЛД50 повышает концентрацию общего белка в сыворотке крови животных, а в дозе 1/5 от ЛД50 пагубно влияет на поджелудочную железу животных, повышая ее ферментативную активность. Уровень глюкозы, концентрация мочевины в сыворотке у подопытных животных была повышенной, как и активность аспартат- и аланинаминотрансферазы, щелочной фосфатазы. Все это указывает на гепатотоксическое действие препарата на крыс, вызывающее угнетение гуморальных факторов неспецифического иммунитета.
Литература
1. Государственная фармакопея. – Т. Х1, Вып. 2. – М.,1968. – С. 182.
2. Козлов С. А., Мусаев М. Б., Михайлицин Ф. С. и др. Изучение острой токсичности митранокса. // Мед. паразитол. и паразит. бол. – 2013. – № 3. – С. 47–48.
3. Козлов С. А., Мусаев М. Б. Антигельминтная эффективность и титрация терапевтических доз отечественного антигельминтика митранокса при мониезиозе и нематодозах овец. // Российский паразитологический журнал. – 2014. – № 2. – С. 87–91.
4. Козлов С. А., Мусаев М. Б., Михайлицин Ф. С. и др. Экспериментальное изучение кумулятивных свойств нового препарата митранокса. // Мед. паразитол. и паразит. бол. – 2013. – № 3. – С. 53–55.
5. Козлов С. А., Мусаев М. Б. Оценка раздражающего действия митранокса и надината на слизистую глаз. // Матер. докл. науч. конф. Всерос. о-ва гельминтол. РАН «Теория и практика борьбы с паразитарными болезнями». – 2014. – Вып. 15. – С.109–110.
6. Козлов С. А., Мусаев М. Б. Параметры острой накожной токсичности и раздражающего действия митранокса и надината. // Матер. докл. науч. конф. Всерос. о-ва гельминтол. РАН «Теория и практика борьбы с паразитарными болезнями». – 2014. – Вып. 15. – С. 110–112.
7. Методические указания по гигиенической оценке новых пестицидов. – Киев, 1988. – С. 32–35.
8. Дыбан А. П., Баранов В. С., Акимова И. М. // Арх. анатом. гистол. эмбриол. – 1970. – Т. 59, № 10. – С. 89–100.
9. Правила лабораторной практики в Российской Федерации: Приказ министерства здравоохранения РФ, № 708н от 23.08.2010.
10. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. Р. У. Хабриева. – Москва: Медицина, 2005.
11. Михайлицын Ф. С., Архипов И. А. и др. Патент №2481327 по заявке
№ 2011153482/04, 27.12.2011, публикация от 10.05.2013 г., Бюл. №13.
© 2015 The Author(s). Published by All-Russian Scientific Research Institute of Fundamental and Applied Parasitology of Animals and Plants named after K.I. Skryabin.
This is an open access article under the Agreement of 02.07.2014 (Russian Science Citation Index (RSCI)) and the Agreemnt of 12/06/2014 (CABI org / Human Sciences section)